Реальний профіль безпеки статинів: результати нового аналізу зв’язку між терапією статинами й побічними ефектами з інструкцій щодо застосування препаратівРезюме. У статті представлено результати нового масштабного метааналізу рандомізованих досліджень статинів. Мета аналіз показав, що, крім раніше описаного зростання ризику м'язових симптомів і нових випадків цукрового діабету, статини пов'язані лише з незначним абсолютним ризиком погіршення результатів функціональних проб печінки, а також із ризиками зміни складу сечі та розвитку набряків невідомої клінічної значущості. Зв'язок між статинами та іншими 62 побічними ефектами, переліченими в інструкціях із застосування, не виявлений. У сучасній медицині гіполіпідемічна терапія статинами застосовується як основний компонент первинної та вторинної профілактики атеросклеротичних серцево-судинних (СС) захворювань у широкого кола пацієнтів. Підставою для використання такого підходу стали результати масштабних рандомізованих плацебо-контрольованих клінічних досліджень (РКД), які показали, що статинотерапія (СТ) знижує ризик серйозних судинних подій [1–5] без збільшення смертності від захворювань, не пов'язаних із судинами [1], або ризику розвитку ракових пухлин [6]. Розрахунки показали, що абсолютна користь у вигляді запобігання серйозним СС подіям від 5-річної ефективної СТ (наприклад, аторвастатином у дозі 40 мг на день) становить 10 і 5% для вторинної та первинної СС профілактики відповідно [7]. Основними встановленими побічними ефектами статинів є порушення з боку м'язів – міопатія (рідко, 1 випадок на 10 000 людино-років [ЛР]) і рабдоміоліз (дуже рідко, приблизно 2–3 випадки на 100 000 ЛР), а також менш виражені м'язові симптоми, частота реєстрації яких дещо (приблизно на 1%) збільшується протягом першого року лікування [8, 9]. Також раніше був доведений зв'язок між прийманням статинів і помірним дозозалежним збільшенням ризику de novo розвитку цукрового діабету (ЦД), яке, однак, переважно спостерігається серед осіб, що мали ознаки переддіабету до початку СТ [10]. Загалом, є підстави вважати, що доведена користь статинів для СС системи значно переважає відомі ризики СТ [8]. Проте дані досліджень, відмінних від РКД, і звіти, отримані в рамках післяреєстраційного спостереження за безпекою, свідчать, що на тлі приймання статинів відзначалося підвищення ризику низки інших побічних ефектів, таких як порушення функції печінки, депресія, порушення когнітивних функцій, порушення сну, гостре ураження нирок або ниркова недостатність, інтерстиціальне захворювання легень і панкреатит. Відомо, що такі фармакоепідеміологічні дані можуть бути корисними для виявлення рідкісних, але клінічно значущих побічних ефектів, однак на них не можна покладатися при оцінці причинно-наслідкового зв'язку між препаратом і більш поширеними в досліджуваній популяції небажаними явищами (НЯ) [7]. Тим не менш, численні НЯ, зареєстровані в ході цих спостережень, були зазначені в інструкціях щодо медичного застосування статинів у розділі «Побічні ефекти», що негативно впливає на оцінку пацієнтами й лікарями співвідношення «користь/ризик» СТ і підвищує ймовірність відмови від застосування або дострокового припинення приймання статинів із наслідками, потенційно небезпечними для життя та здоров'я. Наприклад, після публікації у 2012–2013 роках некоректних тверджень про те, що статини викликають побічні ефекти приблизно в п'ятої частини пацієнтів, у Великій Британії було зафіксовано приблизно 10% зростання кількості пацієнтів, які припинили СТ, призначену для вторинної або первинної СС профілактики, а також зменшення кількості пацієнтів, які проходили оцінку СС ризику для визначення показань до СТ [11]. За підрахунками, протягом наступного десятиліття ці зміни могли призвести до розвитку приблизно 2–6 тис. СС подій, яких можна було б уникнути за допомогою статинів. Подібні дані надходили й з інших країн [12, 13]. У прагненні виправити цю ситуацію група Cholesterol Treatment Trialists' Collaboration (СТТС) провела аналіз даних із великомасштабних РКД, щоб перевірити, чи існує між статинами й НЯ, переліченими в інструкціях щодо їх застосування, причинно-наслідковий зв'язок, і тим самим мінімізувати систематичні та випадкові помилки при оцінці ефектів лікування [8].
Методологія метааналізу СТТС До представленого метааналізу увійшли дані окремих учасників РКД статинів, які проводила група CTТС. Для включення в аналіз підходили подвійні сліпі дослідження за участю щонайменше тисячі пацієнтів і з тривалістю лікування щонайменше 2 роки, у яких зіставні групи учасників отримували статин чи плацебо, або більш інтенсивну чи менш інтенсивну СТ. Автори зібрали всі індивідуальні дані учасників, що стосуються всіх НЯ (незалежно від того, чи вважався статин їхньою причиною), зареєстрованих протягом запланованого періоду лікування та подальшого спостереження в цих дослідженнях. Досліджуваними статинами були аторвастатин, розувастатин, симвастатин, правастатин і флувастатин. Перелік НЯ, чий зв'язок зі статинами планувалося оцінювати, отримали в результаті аналізу розділів «Побічні ефекти» відповідних загальних характеристик лікарських препаратів (ЗХЛП). У результаті було отримано 66 НЯ (тобто 66 потенційних побічних ефектів) [8]. Аналіз цих 66 НЯ проводили за принципом intention-totreat (ITT), тобто з урахуванням призначеного під час рандомізації, а не фактично отриманого лікування (метод мінімізації систематичної помилки). Для кожного НЯ в рамках кожного включеного дослідження розраховували різницю між спостережуваною (o – observed) і очікуваною (e – expected) кількістю подій (о - е), а також показник дисперсії (v, показує «вагу» або надійність цих даних і залежить від кількості учасників та подій). Потім дані всіх окремих досліджень об'єднували й розраховували загальну різницю «о - е», загальну дисперсію, а також їхнє співвідношення (відношення ризиків, RR) і відповідні 95% довірчі інтервали (ДІ). З огляду на велику кількість (66) перевірених НЯ, для мінімізації ризику хибнопозитивних результатів (тобто випадкової «статистичної значущості») автори використовували метод подвійного контролю хибнопозитивних результатів (False Discovery Rate, FDR). Після цього аналізу статистично значущими вважалися лише результати зі значенням FDR <5%, в іншому випадку (при FDR ≥5%) результат вважався незначущим навіть при значенні р<0,05. І, нарешті, для оцінки залежності ефектів від дози проводилося додаткове порівняння стратегій більш інтенсивної та менш інтенсивної СТ. Для результатів із FDR <5% також проводили аналіз у підгрупах з урахуванням вихідних характеристик пацієнтів, конкретного дослідження та тривалості спостереження [8].
Результати метааналізу СТТС До аналізу увійшли 19 подвійних сліпих РКД, у яких один із режимів приймання статинів (у 1 РКД – низькоінтенсивний, у 16 – помірноінтенсивний і у 2 – високоінтенсивний) порівнювали з плацебо. У цих дослідженнях взяли участь 123 940 пацієнтів, медіана періоду спостереження становила 4,5 року (міжквартильний розмах [МКР] 3,1–5,4), середній вік учасників – 63 роки (стандартне відхилення [СВ] 9), 72% (89 407) учасників були чоловіками, 28% (34 533) – жінками, у 48% (59 610) в анамнезі було СС захворювання і у 18% (22 925) – ЦД. Також були доступні дані щодо окремих учасників із чотирьох подвійних сліпих РКД, у яких порівнювали більш інтенсивні та менш інтенсивні режими приймання статинів. У цих 4 дослідженнях взяли участь 30 724 пацієнти, медіана періоду спостереження становила 5,0 років (МКР 2,3–6,6), середній вік – 62 роки (СВ 10), у всіх учасників були СС захворювання [8]. Порівняно з плацебо, для 62 із 66 досліджуваних НЯ призначення статинів не було пов'язано, а для 4 – було пов'язано зі значним надлишковим ризиком (табл.) [8]. До 4 результатів, для яких спостерігався значний надлишковий ризик із FDR <5%, належали аномальні рівні печінкових трансаміназ (0,30% на рік у групі статинів vs 0,22% на рік у групі плацебо; RR 1,41; 95% ДІ 1,26–1,57; p<0,0001; абсолютний щорічний приріст 0,09%), інші відхилення в результатах функціональних печінкових проб (ФПП) (зокрема аномальні рівні лужної фосфатази [ЛФ], аномальні рівні гамма-глутамілтрансферази [ГГТ] і неспецифічні відхилення від норми в результатах ФПП; 0,25 vs 0,20% на рік відповідно; RR 1,26; 95% ДІ 1,12–1,41; p=0,00010; абсолютний щорічний приріст 0,05%), зміна складу сечі (0,21 vs 0,18% на рік відповідно; RR 1,18; 95% ДІ 1,04–1,33; p=0,0089; абсолютний щорічний приріст 0,03%) і набряки (1,38 vs 1,31% на рік відповідно; RR 1,07; 95% ДІ 1,02–1,12; p=0,0071; абсолютний щорічний приріст 0,07%) [8]. Для обох указаних побічних ефектів із боку печінки найбільша різниця між статином і плацебо, а також між більш інтенсивною та менш інтенсивною СТ спостерігалася в дослідженнях із застосуванням аторвастатину в дозі 80 мг/добу. Після виключення цих досліджень із набору даних аналіз решти РКД показав зіставне збільшення ризиків порушень із боку печінки при використанні всіх досліджуваних режимів СТ порівняно з плацебо й усіх варіантів більш інтенсивної СТ порівняно з менш інтенсивною СТ [8]. Аналіз окремих компонентів комбінованого побічного ефекту «інші відхилення в результатах ФПП» показав зіставне підвищення ризиків для компонентів «аномальні рівні ЛФ» (RR 1,18; 95% ДІ 0,86–1,62) та «аномальні рівні ГГТ» (RR 1,21; 95% ДІ 0,95–1,55) і дещо більший відносний ризик для компонента «неспецифічні відхилення від норми в результатах ФПП» (RR 1,28; 95% ДІ 1,12–1,46) при застосуванні статинів порівняно з плацебо й загалом аналогічну картину при застосуванні більш інтенсивної порівняно з менш інтенсивною СТ. Даних про те, що статини підвищують ризик клінічно значущих гепатобіліарних ускладнень, зокрема холестазу, жовтяниці, печінкової недостатності, ураження печінки, гепатиту або стеатозу печінки, не виявлено (табл.) [8]. Аналіз окремих компонентів комбінованого побічного ефекту «зміни складу сечі» показав підвищення ризику комбінації «протеїнурія / альбумінурія / мікроальбумінурія» (RR 1,20; 95% ДІ 1,02–1,42; абсолютний щорічний приріст 0,02%), але не виявив явного впливу СТ на збільшення кількості лейкоцитів або еритроцитів у сечі й частоту виявлення інших відхилень у результатах аналізу сечі. Порівняння ефектів більш інтенсивної та менш інтенсивної СТ не виявило значного (за FDR) підвищення ризику зміни складу сечі в пацієнтів, які отримували більш інтенсивну СТ. Також не було виявлено значущої (за FDR) тенденції або гетерогенності даних за цим показником із різних РКД, у яких різні за інтенсивністю режими СТ порівнювали з плацебо. Ознак впливу статинів на інші клінічно значущі ниркові наслідки й зміни складу сечі, у тому числі гостре ураження нирок, дизурію, гематурію та порушення сечовипускання, не виявлено (табл.) [8]. Аналогічний аналіз даних щодо побічного ефекту «набряк» не виявив різниці між більш інтенсивною та менш інтенсивною СТ і не визначив значущої (за FDR) тенденції або гетерогенності даних за цим показником у різних РКД, у яких порівнювали режими СТ різної інтенсивності з плацебо. Значного впливу статинів на ризик розвитку інших порушень загального характеру, зокрема астенії, втоми, нездужання, болю та лихоманки, також не виявлено (табл.) [8]. Для решти 62 НЯ порівняння статинів із плацебо й більш інтенсивної СТ з менш інтенсивною СТ із використанням FDR не виявили значного підвищення ризику.
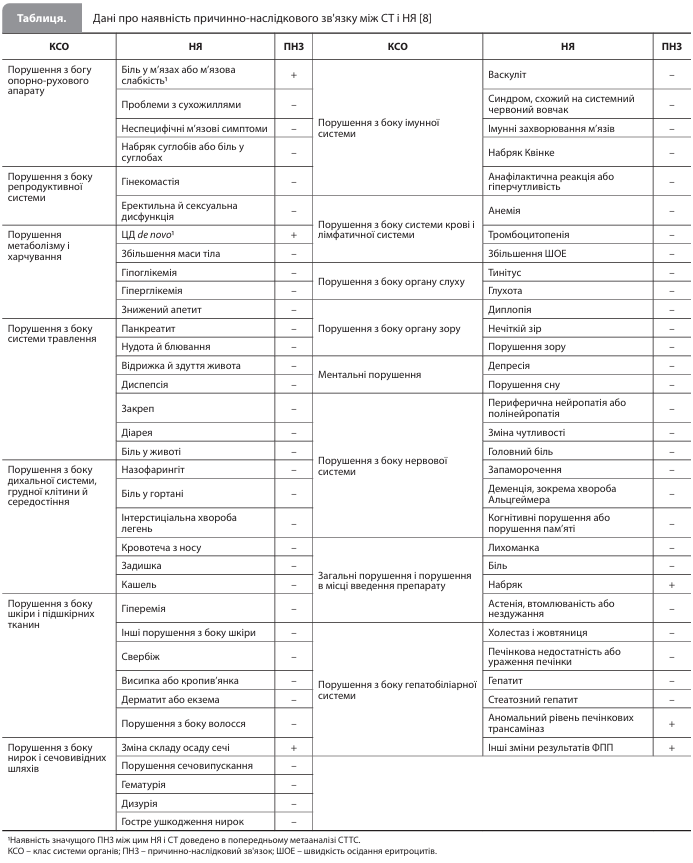
Обговорення результатів метааналізу СТТС Отже, проєкт CTT Collaboration після аналізу величезного масиву даних учасників РКД показав, що, окрім зазначеного раніше значного підвищення ризику м'язових симптомів [9] і розвитку ЦД [10], у статинів є лише чотири додаткові побічні ефекти: аномальні рівні печінкових трансаміназ, інші відхилення в результатах ФПП, зміна складу сечі й набряки. При цьому причинно-наслідковий зв'язок між прийманням статинів і переважною більшістю побічних ефектів, зазначених в інструкціях щодо їх застосування (зокрема порушення сну, втрата пам'яті, сексуальна дисфункція, депресія та інтерстиціальні захворювання легень), відсутній. З огляду на ці результати, автори дійшли висновку, що частина інформації, представлена в інструкціях щодо застосування статинів, є недостовірною та може вводити в оману [8]. Автори метааналізу підкреслюють, що виявлений вплив СТ на рівні печінкових ферментів був особливо очевидним при застосуванні аторвастатину в дозі 80 мг на добу (максимальна доступна доза аторвастатину), що узгоджується з даними попередніх досліджень [14] та уявленням про дозозалежний вплив СТ на результати ФПП. Водночас зв'язок між СТ і розвитком серйозних печінкових ускладнень, таких як холестаз, жовтяниця, печінкова недостатність, ураження печінки та гепатит, не виявлений. Це узгоджується з даними більш раннього метааналізу, який не виявив доказів несприятливого впливу СТ на захворюваність раком печінки або смертність від гепатоцелюлярного раку [6]. Наразі проводяться подальші дослідження, присвячені більш детальній оцінці клінічної значущості змін результатів ФПП і, зокрема, підвищення рівня трансаміназ, при застосуванні статинів, для розробки більш інформативних рекомендацій щодо моніторингу цих показників під час СТ [15–18]. Клінічна значущість інформації щодо зміни складу сечі та набряків невідома, з огляду, зокрема, на відсутність ознак дозозалежності. Загалом, доведено, що СТ може незначно підвищувати концентрацію білка в сечі без істотного впливу на інші ниркові наслідки (у тому числі на ризик гострого ураження нирок). Інформація, включена до бази даних СТТС, не дозволила встановити ступінь тяжкості набряків у пацієнтів, які приймали СТ у РКД, однак спостережуване невелике збільшення рівня білка в сечі навряд чи є причиною зростання цього ризику. Вважається, що терапія статинами запобігає або уповільнює розвиток серцевої недостатності за рахунок зниження частоти ішемічної хвороби серця та подальшого ураження серця [19–21], що робить зв'язок підвищеного ризику набряків із серцевою недостатністю також малоймовірним. Серед НЯ, для яких зв'язок із СТ не був доведений, автори звертають особливу увагу на когнітивні порушення. Цей висновок підтверджують результати більш детальних оцінок зв'язку між прийманням статинів і когнітивними порушеннями, проведених у дослідженнях PROSPER [22] та HPS [23].
Висновок Проведений групою СТТС метааналіз даних окремих учасників 23 подвійних сліпих РКД, що охопили понад 150 тис. пацієнтів, показав, що терапія статинами збільшує ризик підвищення рівнів печінкових трансаміназ та інших показників функції печінки залежно від інтенсивності режиму, хоча абсолютні надлишкові ризики й клінічні наслідки цих ефектів, як видається, невеликі. При цьому для переважної більшості (62 із 66) інших НЯ, перелічених в інструкціях із застосування статинів як потенційні побічні ефекти лікування, ознак причинно-наслідкового зв'язку з прийманням статинів не виявлено. Ці результати підтверджують думку про те, що користь від СТ переважає будь-які пов'язані з нею ризики, і вказують на необхідність перегляду тексту інструкцій із застосування статинів та оновлення інших офіційних джерел медичної інформації, що дозволить лікарям і пацієнтам ухвалювати обґрунтовані рішення щодо балансу користі та ризиків статинотерапії.
Список літератури знаходиться в редакції
Автор огляду Галина Мілюхина Medicine Review 2026; 2 (91): 5 |
Корисні посилання






|
|
Інформація, розміщена на сайті, призначена тільки для професіоналів охорони здоров'я та не може бути використана як інструкція для самолікування. |
Головна | Про видання | Поточний номер | Архів номерів | Новини | Правова інформація
Medicine Review © 2008—2026. Усі права захищені.
|
мапа сайту корисні посилання |