Вибір іP2Y12 для монотерапії після гострого коронарного синдрому: результати нового метааналізу рандомізованих досліджень клопідогрелю та тикагрелоруРезюме. У статті представлено новий метааналіз семи рандомізованих клінічних досліджень, присвячених оцінці результатів раннього (до 3 місяців після гострого коронарного синдрому [ГКС]) переходу з подвійної антитромбоцитарної терапії (ПАТ) на монотерапію інгібітором P2Y12-рецепторів тромбоцитів (iP2Y12) порівняно зі стандартною 12-місячною ПАТ. Аналіз охопив дані більш ніж 27 тис. пацієнтів і був стратифікований з урахуванням використовуваного іP2Y12. Результати показали, що стратегія переходу на монотерапію іP2Y12 після короткої ПАТ знижує ризик кровотеч без шкоди для протиішемічної ефективності порівняно з 12-місячною ПАТ і що перехід на монотерапію тикагрелором має перевагу перед переходом на монотерапію клопідогрелем. Ключові моменти: 1. 12-місячна ПАТ є стандартом лікування пацієнтів, які перенесли ГКС, проте тривале комбіноване використання антиагрегантів може збільшувати геморагічний ризик до ступеня, що нівелює користь від зниження ризику ішемічних подій. 2. Після вдосконалення методик черезшкірного коронарного втручання, у тому числі впровадження в практику сучасних стентів із лікарським покриттям, з’явилася потреба в альтернативних антиагрегантних стратегіях, що дозволяють знизити ризик кровотеч без збільшення ризику ішемічних подій порівняно зі стандартною річною ПАТ. 3. Метааналіз даних семи сучасних рандомізованих клінічних досліджень, присвячених порівнянню ефектів стратегії раннього переходу з ПАТ на монотерапію іP2Y12 з ефектами продовження ПАТ протягом 12 місяців, показав, що такий перехід знижує ризик кровотеч без втрати протиішемічного захисту, при цьому кращі результати досягаються в разі, якщо в якості іP2Y12 для монотерапії використовується тикагрелор, а не клопідогрель. У хворих із гострим коронарним синдромом (ГКС) стандартним методом лікування та профілактики ішемічних подій є річна подвійна антиагрегантна терапія (ПАТ) комбінацією ацетилсаліцилової кислоти (АСК) і потужного інгібітора P2Y12-рецепторів тромбоцитів (іP2Y12: тикагрелор або прасугрель) [1]. Проте, як показує практика, переваги такої ПАТ можуть нівелюватися збільшенням ризику кровотеч – ускладнення, що підвищує ризик смерті [2]. Відомо, що, спочатку (тобто протягом 1–3 місяців після ГКС та/або черезшкірного коронарного втручання [ЧКВ]) ризик ішемічних подій є високим, але згодом він поступово знижується, тоді як ризик кровотеч, як правило, залишається стабільним тривалий час після ГКС [3]. Для підвищення безпечності антиагрегантної терапії без шкоди для її ефективності були розроблені стратегії деескалації ПАТ, мета яких – збалансувати геморагічний та ішемічний ризики [4]. Перша стратегія деескалації, впроваджена в клінічну практику, передбачала скорочення ПАТ шляхом скасування іP2Y12 через 3–6 місяців після ГКС із переходом на монотерапію АСК [3, 4]. Однак через збільшення кількості ішемічних подій порівняно зі стандартною 12-місячною ПАТ, особливо у хворих на ГКС [5, 6], цю стратегію рекомендується застосовувати лише у відібраних пацієнтів із високим ризиком кровотеч [1]. «Дзеркальна» стратегія з раннім скасуванням АСК і подальшою монотерапією іP2Y12 також була протестована й показала у цілому більш обнадійливі результати [7–10]. Проте питання щодо того, який із сучасних пероральних іP2Y12 (клопідогрель vs прасугрель vs тикагрелор) зможе забезпечити кращий профіль безпечності й ефективності антиагрегантної монотерапії після короткострокової ПАТ, залишається відкритим. Дослідженню цієї проблеми був присвячений метааналіз рандомізованих контрольованих досліджень (РКД) стратегії переходу на монотерапію іP2Y12 після короткого (≤3 місяців) курсу ПАТ у пацієнтів із ГКС, який порівняв результати такого переходу з результатами стандартної 12-місячної ПАТ з урахуванням іP2Y12 (тикагрелор або клопідогрель), що використовувався в групі монотерапії (метааналіз Galli et al.) [11]. Основна інформація про це дослідження стисло подана в огляді.

Методологія метааналізу Galli et al. Пошук РКД проводився в базах даних MEDLINE, PubMed, Cochrane і Web of Science; період пошуку – із січня 2009 по червень 2024 року. Критеріям пошуку відповідали РКД, у яких: 1) учасниками були пацієнти з ГКС, які перенесли ЧКВ з імплантацією стента з лікарським покриттям; 2) проводилася рандомізація учасників у групу стандартної 12-місячної ПАТ або групу переходу на монотерапію іP2Y12 після початкової короткої ПАТ; 3) реєструвалася як мінімум одна значуща для Galli et al. кінцева точка [11]. Дослідження за участю пацієнтів, які мали показання до пероральної антикоагулянтної терапії або використовували інші (не іP2Y12) антиагрегантні препарати, в аналіз не включалися. Для аналізу збиралися такі дані: особливості дизайну дослідження, тривалість спостереження, основні клінічні характеристики пацієнтів, параметри проведених процедур та інформація про кінцеві точки (визначення і результати оцінки). Первинною кінцевою точкою метааналізу була комбінація «основні несприятливі серцево-судинні (СС) події (MACE)». Вторинними кінцевими точками були: смерть від будь-яких причин, комбінація «всі несприятливі клінічні події (net adverse clinical events – NACE)», а також окремі ішемічні (СС смерть, інфаркт міокарда [ІМ], інсульт, тромбоз стента) і геморагічні (будь-яка кровотеча, велика кровотеча) кінцеві точки [11]. Спочатку автори оцінювали результати раннього переходу з ПАТ на монотерапію iP2Y12 порівняно зі стандартною ПАТ за допомогою об'єднаного аналізу всіх включених РКД, а потім – за допомогою аналізу підгруп досліджень, виділених з урахуванням iP2Y12, що застосовувався в групі монотерапії. Для кожної кінцевої точки розраховували відношення ризиків (ВР) і 95% довірчий інтервал (ДІ), а також оцінювали якість доказів. Для перевірки отриманих результатів автори провели серію аналізів чутливості. Щоб визначити результати як переконливі або непереконливі (тобто з'ясувати, чи достатньо переконливою є оцінка ефекту терапії на конкретну кінцеву точку, щоб на цю оцінку не могли вплинути подальші дослідження), автори виконали послідовний аналіз досліджень з оцінкою кожної кінцевої точки в загальній вибірці РКД і в кожній із двох підгруп досліджень [11].
Результати метааналізу Galli et al. Пошук, проведений у базах даних, дозволив відібрати сім РКД за участю загалом 27 284 пацієнтів (табл.) [12–18]. У п'яти дослідженнях монотерапію тикагрелором порівнювали з ПАТ на основі тикагрелору [12–16], у двох – монотерапію клопідогрелем порівнювали з ПАТ на основі клопідогрелю [17, 18]. У чотирьох дослідженнях вивчали ефекти переходу на монотерапію іP2Y12 після в середньому 1 місяця ПАТ (у двох РКД – 1 місяць, в одному – <1 місяця, в одному – 1–2 місяці), а в трьох – після 3-місячної ПАТ. Середня тривалість ПАТ у групі монотерапії іP2Y12 становила 51 день [11].
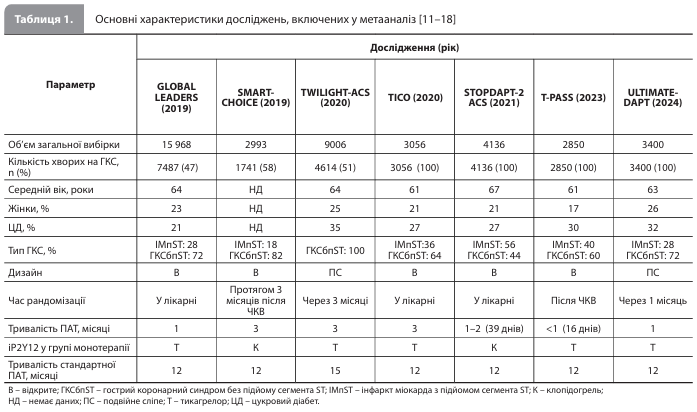
Порівняння груп лікування (монотерапія іР2Y12 vs 12-місячна ПАТ) за демографічними й процедурними характеристиками показало відсутність істотних розбіжностей. У досліджуваній вибірці середньозважений вік становив 63,5 року, частка жінок – 22,5%, частка пацієнтів із цукровим діабетом – 27,7% [11]. Об'єднаний аналіз даних семи РКД не виявив розбіжностей між групою переходу з короткої ПАТ на монотерапію іP2Y12 і групою 12-місячної ПАТ за частотою МАСЕ (ВР 0,92; 95% ДІ 0,76–1,12; р=0,424), хоча якість доказів була визнана низькою. Натомість аналіз у підгрупах, виділених з урахуванням іP2Y12, що використовувався в групі монотерапії, виявив наявність значущої взаємодії (р для взаємодії = 0,016) між ефектом і типом іP2Y12, продемонструвавши значне зниження частоти МАСЕ в дослідженнях монотерапії тикагрелором (ВР 0,84; 95% ДІ 0,71–0,98; р=0,028), але не в дослідженнях монотерапії клопідогрелем (ВР 1,32; 95% ДІ 0,94–1,84; р=0,105) (рис.) [11]. Якість доказів оцінювалася як середня для монотерапії тикагрелором і дуже низька для монотерапії клопідогрелем [11]. Аналіз NACE й смертності від будь-яких причин показав такі результати. В об'єднаному аналізі семи РКД перехід на монотерапію іP2Y12 після короткої ПАТ був пов'язаний зі значним зниженням частоти NACE (ВР 0,75; 95% ДІ 0,60–0,94; р=0,011) і незначним зниженням частоти смерті від будь-яких причин порівняно з 12-місячною ПАТ. Водночас, як і у випадку з МАСЕ, спостерігалася залежність ефекту від типу використовуваного іP2Y12 (р для взаємодії: 0,042 – для смерті від будь-яких причин, 0,018 – для NACE). Тобто було показано, що зниження NACE і смертності від будь-яких причин було значущим при використанні тикагрелору (ВР 0,70 [95% ДІ 0,58–0,84; р<0,001] і 0,77 [95% ДІ 0,61–0,98; р=0,035] відповідно), але не при використанні клопідогрелю (ВР 1,16 [95% ДІ 0,79–1,63; р=0,487] і 1,49 [95% ДІ 0,80–2,69; р=0,179] відповідно) (рис.). В обох аналізах і для обох кінцевих точок якість доказів оцінювалася як середня [11]. Аналіз окремих ішемічних кінцевих точок показав такі результати. Згідно з об'єднаним аналізом, перехід на монотерапію іP2Y12 після короткої ПАТ не був пов'язаний із підвищеним ризиком ішемічних подій порівняно з 12-місячною ПАТ. Водночас було виявлено значущу взаємодію між ризиком ІМ і типом використовуваного іP2Y12 (р для взаємодії = 0,028), що проявлялося незначним зниженням ризику ІМ у підгрупі тикагрелору й підвищеним ризиком ІМ у підгрупі клопідогрелю (ВР 1,87; 95% ДІ 1,05–3,32; р=0,034) (рис.) [11]. У рамках об'єднаного аналізу якість доказів була високою для СС смерті, низькою для ІМ і середньою для інших ішемічних кінцевих точок. У підгрупі монотерапії тикагрелором якість доказів була високою для СС смерті й середньою для інших ішемічних кінцевих точок, натомість у підгрупі монотерапії клопідогрелем якість доказів була середньою для всіх ішемічних кінцевих точок [11]. Аналіз геморагічних кінцевих точок показав такі результати. За даними об'єднаного аналізу, перехід на монотерапію іP2Y12 після короткої ПАТ був пов'язаний зі значним зниженням частоти будь-яких кровотеч (ВР 0,54; 95% ДІ 0,43–0,66; р<0,001) і частоти великих кровотеч (ВР 0,47; 95% ДІ 0,37– 0,60; р<0,001). Водночас, згідно з аналізом у підгрупах, ефект переходу на монотерапію іP2Y12 на ризик кровотеч порівняно з 12-місячною ПАТ не залежав від типу іP2Y12 (рис.) [11]. Значення ВР для будь-яких кровотеч і великих кровотеч становили: монотерапія тикагрелором – 0,54 (95% ДІ 0,43–0,69; р<0,001) і 0,47 (95% ДІ 0,36–0,62; р<0,001) відповідно; монотерапія клопідогрелем – 0,49 (95% ДІ 0,30–0,78; р=0,003) і 0,41 (95% ДІ 0,20–0,83; р=0,013) відповідно (рис.). У рамках об'єднаного аналізу якість доказів була визнана низькою для будь-яких кровотеч і середньою для великих кровотеч. Проте в підгрупі монотерапії тикагрелором якість була середньою, а в підгрупі монотерапії клопідогрелем – низькою для обох геморагічних кінцевих точок. Послідовний аналіз досліджень підтвердив переконливість доказів більшої безпечності стратегії переходу на монотерапію іP2Y12 після короткої ПАТ порівняно з 12-місячною ПАТ. Загалом, аналіз переконливості доказів користі показав, що дані про кровотечі переконливо свідчать про користь такого переходу, дані про МАСЕ переконливо свідчать про відсутність користі, і що для остаточних висновків щодо інших ішемічних кінцевих точок необхідні додаткові дані. Аналіз досліджень ефектів монотерапії клопідогрелем порівняно з 12-місячною ПАТ не виявив переконливих доказів користі переходу на монотерапію цим іP2Y12. Водночас докази зниження частоти NACE і будь-яких кровотеч порівняно з 12-місячною ПАТ, отримані з досліджень монотерапії тикагрелором, були визнані переконливими, а для остаточних висновків щодо впливу тикагрелору на інші кінцеві точки, згідно з результатами аналізу, необхідні додаткові дані [11]. Аналіз чутливості показав результати, які в цілому відповідають результатам основного аналізу, як і аналіз, проведений після виключення РКД, що зробили найбільший внесок у гетерогенність даних (STOPDAPT-2 ACS, T-PASS і GLOBAL LEADERS) [11].
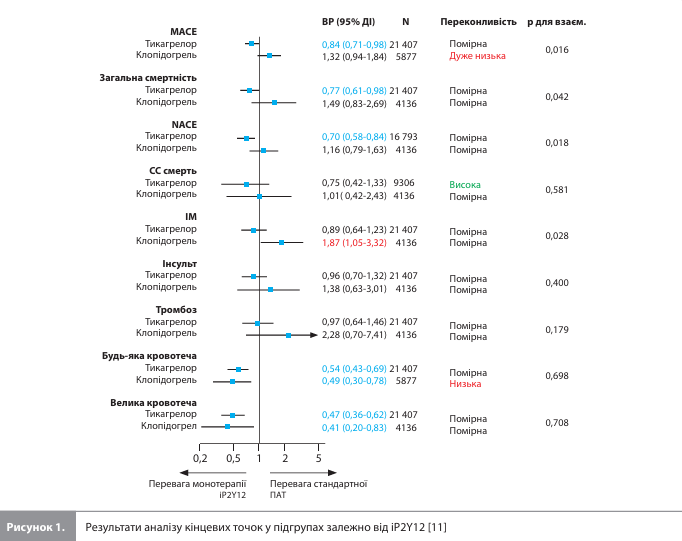
Обговорення результатів метааналізу Galli et al. Результати представленого метааналізу можна резюмувати в такий спосіб [11]: 1. Загалом, стратегія переходу на монотерапію іP2Y12 після короткої ПАТ знижує ризик кровотеч без впливу на ризики ішемічних подій у пацієнтів із ГКС; 2. Монотерапія клопідогрелем і монотерапія тикагрелором по-різному впливають на результати: тикагрелор асоціюється з кращими результатами, ніж клопідогрель; 3. Порівняно зі стандартною 12-місячною ПАТ монотерапія клопідогрелем знижує ризик будь-яких кровотеч і ризик великих кровотеч, але пов'язана зі зростанням ризику ІМ і не має переваг щодо впливу на ризики МАСЕ й NACE; 4. Монотерапія тикагрелором, як і монотерапія клопідогрелем, знижує ризики будь-яких і великих кровотеч, проте на відміну від монотерапії клопідогрелем може знизити смертність і ризик MACE, а також переконливо знижує ризик NACE порівняно з 12-місячною ПАТ. Представлений метааналіз має низку переваг перед іншими дослідженнями такого типу, оскільки в ньому враховуються важливі фактори, що впливають на оцінку безпечності й ефективності монотерапії іP2Y12 порівняно зі стандартною 12-місячною ПАТ у специфічному контексті ГКС. Зокрема, Galli et al. використовували тільки дані пацієнтів, які перенесли ГКС (тоді як у багатьох попередніх дослідженнях брали участь пацієнти як із гострим, так і з хронічним коронарним синдромом), враховували расу пацієнтів (багато попередніх досліджень були зосереджені на пацієнтах зі Східної Азії, для яких типовим є високий ризик кровотеч і низький ризик ішемії порівняно з іншими етнічними групами, що перешкоджає перенесенню результатів на загальну популяцію), а також, що найважливіше, стратифікували оцінку стратегії переходу на монотерапію іP2Y12 за типом іP2Y12 (потужний іP2Y12 тикагрелор або менш потужний клопідогрель, доведено пов'язаний із великою варіабельністю фармакологічної відповіді, що призводить до високої реактивності тромбоцитів і подальшого підвищення ішемічного ризику майже у 30% пацієнтів [11, 19]). Тому результати, отримані Galli et al., краще застосовні до реальної клінічної практики. Крім того, до порівняння стратегій (рання деескалація vs стандартна ПАТ) уперше були включені останні дані досліджень T-PASS та ULTIMATE DAPT, які розширюють докази на користь переходу на монотерапію тикагрелором на випадки скасування ПАТ менш ніж через місяць після ГКС [20, 21]. Додатково Galli et al. вперше провели послідовний аналіз включених РКД, щоб з'ясувати, чи достатньо переконлива оцінка ефекту терапії на кожен результат, щоб на неї не могли вплинути подальші дослідження. І, нарешті, автори ретельно оцінили якість доказів для кожної досліджуваної кінцевої точки. Основний результат представленого аналізу полягає в тому, що вибір іP2Y12 (тобто клопідогрелю або тикагрелору) для монотерапії значно впливає на результати в пацієнтів із ГКС із групи високого ризику. Було показано, що попри зіставне зниження геморагічного ризику при використанні обох іP2Y12, лише монотерапія тикагрелором забезпечувала зниження ризику ішемічних подій і смерті порівняно зі стандартною ПАТ. Ці результати узгоджуються з даними дослідження STOPDAPT-2 ACS, у якому монотерапія клопідогрелем після 1–2 місяців ПАТ була пов'язана з підвищеним ризиком СС подій порівняно зі стандартною ПАТ після ГКС [18], а також із результатами попередніх метааналізів, які показали значне зниження ризику смерті на тлі монотерапії тикагрелором, але не при використанні інших іP2Y12 [22, 23]. Ці розбіжності були особливо очевидними, коли початкова ПАТ припинялася менш ніж через 3 місяці, і ставали менш вираженими при більш тривалій (3 місяці) ПАТ, що вказує на можливу користь переходу на монотерапію клопідогрелем після більш тривалої початкової ПАТ. Проте послідовний аналіз досліджень показав, що докази на користь монотерапії клопідогрелем на даний момент є недостатніми і мають нижчу якість, ніж докази на користь монотерапії тикагрелором, яких достатньо для остаточного висновку про зниження частоти NACE (тобто про збільшення загальної клінічної користі) порівняно зі стандартною 12-місячною ПАТ [11]. Загалом, результати, представлені Galli et al., мають велике клінічне значення, оскільки підтверджують, що різні фармакологічні властивості різних іP2Y12 приводять до різних співвідношень «користь/ризик», і що якщо в пацієнта з ГКС і без протипоказань обирається стратегія деескалації у вигляді раннього (після короткої ПАТ) переходу на монотерапію іP2Y12, то в такій ситуації, згідно з наявними даними, тикагрелор буде кращим варіантом, ніж клопідогрель [11]. При інтерпретації результатів цього метааналізу потрібно враховувати як низку обмежень, так і ефекти заходів, спрямованих на їх подолання. Основними обмеженнями є відсутність аналізу даних на рівні окремих пацієнтів, що не дозволило глибоко оцінити вплив різних коваріат на загальну оцінку ефектів лікування; дисбаланс у кількості досліджень тикагрелору й клопідогрелю і, відповідно, включених пацієнтів, які отримували тикагрелор і клопідогрель (21 407 і 5877 пацієнтів відповідно); більша частка пацієнтів з ІМ із підйомом сегмента ST у дослідженнях клопідогрелю; а також висока гетерогенність даних із різних включених досліджень за деякими кінцевими точками. Заходом щодо пом'якшення ефектів цих обмежень було проведення аналізів чутливості й аналізів у підгрупах, які показали результати, зіставні з отриманими в основному аналізі. Також автори звертають увагу на те, що крім РКД SMART-CHOICE, у якому невеликий відсоток пацієнтів отримував монотерапію прасугрелем, у дослідженнях, що увійшли в метааналіз, прасугрель не використовувався, що не дозволяє робити висновки про ефекти раннього переходу на монотерапію прасугрелем порівняно зі стандартною 12-місячною ПАТ після ГКС на підставі представлених результатів [11].
Висновки Згідно з результатами метааналізу Galli et al., у пацієнтів із ГКС, які перенесли ЧКВ з імплантацією стента з лікарським покриттям, перехід на монотерапію іP2Y12 після короткої ПАТ знижує ризик кровотеч без шкоди для протиішемічної ефективності порівняно з продовженням ПАТ протягом 12 місяців. При цьому, попри зіставне зниження ризиків кровотеч при використанні клопідогрелю та тикагрелору, профіль протиішемічних ефектів і, як наслідок, показник чистої клінічної користі були більш сприятливими для монотерапії тикагрелором, ніж для монотерапії клопідогрелем. У цілому, представлені результати дозволяють припустити, що при скасуванні АСК після короткої ПАТ у пацієнтів із ГКС монотерапія тикагрелором має перевагу перед монотерапією клопідогрелем.
Список літератури знаходиться в редакції
Автор огляду Олена Грибова Medicine Review 2026; 1 (90): 12 |
Корисні посилання






|
|
Інформація, розміщена на сайті, призначена тільки для професіоналів охорони здоров'я та не може бути використана як інструкція для самолікування. |
Головна | Про видання | Поточний номер | Архів номерів | Новини | Правова інформація
Medicine Review © 2008—2026. Усі права захищені.
|
мапа сайту корисні посилання |